TRACE UM NOVO CURSO PARA SOBREVIDA
EV-201 (Coorte 2)
PADCEV® forneceu uma resposta completa em 22% (n=20/89) dos pacientes e resposta parcial em 28% (n=25/89) dos pacientes14
PADCEV alcançou uma resposta
clinicamente significativa em
pacientes inelegíveis para cisplatina4

O PADCEV apresentou uma
duração mediana de resposta
aproximada de 14 meses1,4
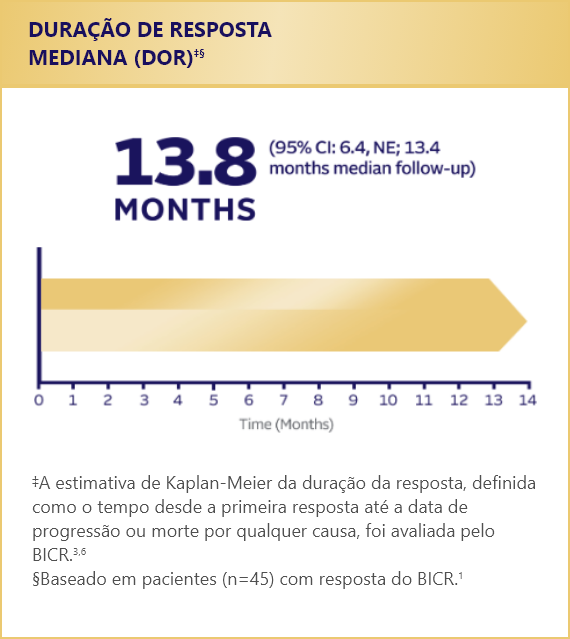
BICR=revisão central independente cega; IC=intervalo de confiança; RC=resposta completa; DOR=duração da resposta; NE=não estimável;
TRO=taxa de resposta objetiva; RP=resposta parcial; RECIST=Critérios de Avaliação de Resposta em Tumores Sólidos.
Informações adicionais EV-201 (Coorte 2)
Alteração nas lesões-alvo de pacientes avaliáveis (n=77)4||
No EV-201, o Endpoint primario taxa de resposta objetiva foi atingido. Assim como o Endpoint secundário tempo de duração de resposta. A taxa de resposta objetiva do estudo (TRO) foi de 51% (n=45/89; IC 95%: 39,8% – 61,3%), sendo 22% resposta completa e 28% resposta parcial de acordo com os critérios Recist 1.1. A DOR mediana foi de 13,8 meses.3
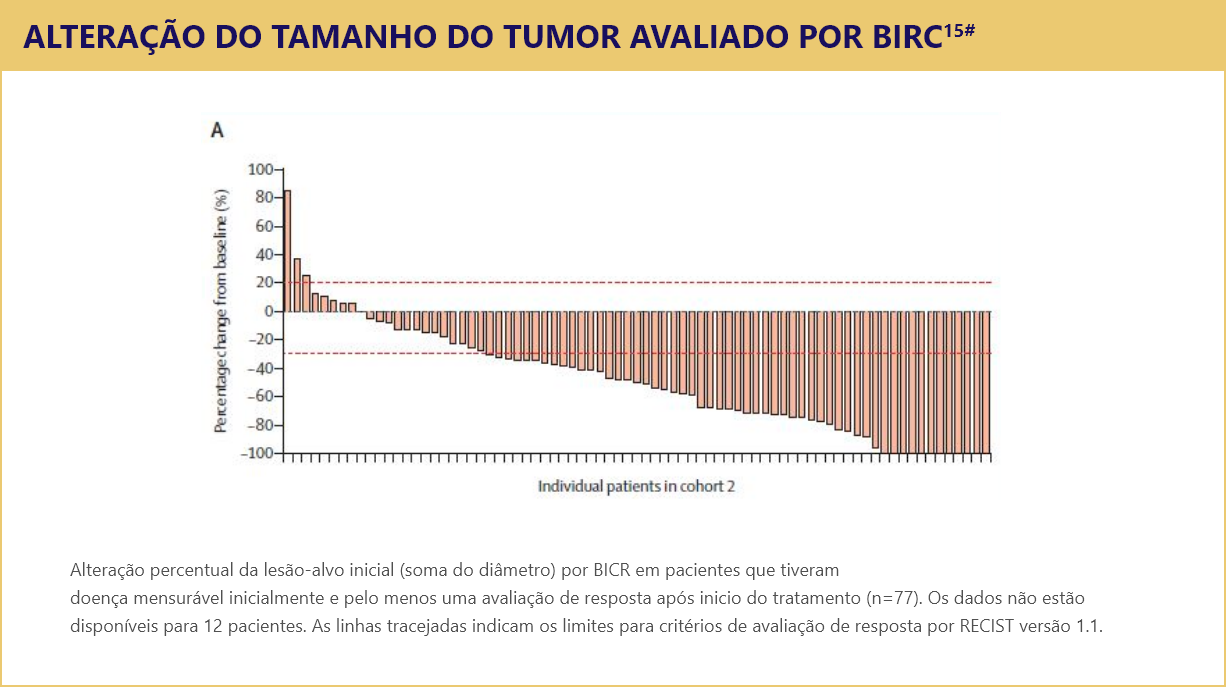
||Os dados não estão disponíveis para 12 indivíduos devido à ausência de avaliação de resposta após a linha de base (n=5), avaliação incompleta das lesões alvo após a linha de base (n=1) ou nenhuma doença mensurável na linha de base por BICR (n=6).15
¶ORR consistiu em CR ou PR confirmado por RECIST v1.1 conforme avaliado pelo BICR. A RC foi definida como o desaparecimento de todas as lesões alvo e não alvo. A PR foi definida como uma diminuição ≥30% na soma dos diâmetros das lesões alvo, tomando como referência a soma dos diâmetros da linha de base.15,19,21
#Redução percentual máxima da linha de base na soma da lesão alvo do diâmetro por BICR em indivíduos que tinham doença mensurável na linha de base e pelo menos uma avaliação de resposta avaliável após a linha de base.15,19
**Pacientes avaliáveis para resposta à lesão-alvo (n=77/89) precisavam ter doença mensurável na linha de base por BICR e avaliação pós-linha de base adequada para as lesões-alvo.15,19
††De acordo com o RECIST v1.1, doença estável foi definida como nem encolhimento suficiente para se qualificar para PR nem aumento suficiente para se qualificar para DP, tomando como referência a menor soma de diâmetros durante o estudo.21
‡‡De acordo com o RECIST v1.1, a doença progressiva foi definida como ≥20% de aumento na soma dos diâmetros das lesões-alvo, tomando como referência a menor soma no estudo (isso inclui a soma da linha de base, se for a menor no estudo). Além do aumento relativo de 20%, a soma também deve demonstrar um aumento absoluto de pelo menos 5 mm. (Observação: o aparecimento de uma ou mais novas lesões também é considerado progressão.)21
Informações adicionais EV-201 (Coorte 2)
Analise de Subgrupo : Taxa de resposta Objetiva4

ECOG PS=Eastern Cooperative Oncology Group performance status; PD-(L)1=receptor de morte programado-1 ou ligante de morte programado.1

